Hemoglobin
Ebben a cikkben részletesen megvizsgáljuk a Hemoglobin-et, kitérve annak fontosságára és a mindennapi élet különböző területein gyakorolt hatásaira. A Hemoglobin alapvető szerepet játszik a mai társadalomban, mivel a személyes döntésektől a kormányzati politikákig mindenre hatással van. A szövegben végig mélyrehatóan megvizsgáljuk az emberek életére gyakorolt hatását, valamint relevanciáját a szakmai és tudományos világban. Elemezni fogjuk az idők folyamán bekövetkezett fejlődését és a technológiai és kulturális fejlődésre gyakorolt hatását is. Átfogó és kritikus megközelítéssel ennek a cikknek az a célja, hogy átfogó és teljes képet adjon a Hemoglobin-ről, lehetővé téve az olvasó számára, hogy világosabban megértse annak fontosságát és hatókörét a mai társadalomban.
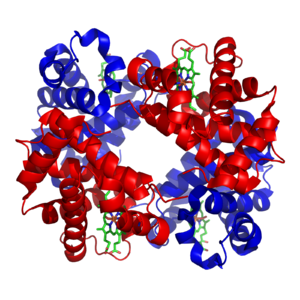
A hemoglobin a gerincesek esetében, a vérben, a vörösvértestekben található vastartalmú oxigéntranszport metalloprotein. Emlősökben ez a fehérje teszi ki a vörösvértestek szárazanyag-tartalmának körülbelül 97%-át, és a vörösvértestek összes anyagának 35%-át (az összanyag-tartalomba a vizet is beleértve). A hemoglobin szállítja az oxigént a tüdőktől vagy kopoltyúktól a test többi részébe, beleértve az izmokat, ahol leadja az oxigént.
A hemoglobin szó a görög haima (αἷμα = vér) és a latin globus (golyó, gömb) összevonásából keletkezett.
Szerkezete
Az emberben a hemoglobin négy alegységből áll. Mindegyiket egy globuláris fehérjerész építi fel, amely szorosan kapcsolódik egy nem-fehérje jellegű hem csoporttal. A hemcsoportban egy Fe2+ található egy porfirin nevű heterociklusos gyűrűben. A Fe2+, amely az oxigént megköti, kötést létesít a gyűrű belsejében található négy nitrogénatommal. A vas a globuláris fehérjével is szoros kapcsolatot létesít, az abban található egyik hisztidin oldalláncában található imidazolgyűrű egyik nitrogénatomján keresztül. A Fe2+-on található hatodik „hely” képes reverzíbilisen megkötni az oxigént. Így a vashoz hat ligandum kapcsolódik, a vas körül oktaéderes a szimmetria. Ha a hemoglobin nem köt oxigént, az oxigén helyét egy gyengén kötött vízmolekula foglalja el. A hemoglobinban a vas töltése +2 (Fe2+) és +3 (Fe3+) is lehet, de a Fe3+-t tartalmazó hemoglobin (methemoglobin) nem képes oxigént kötni.
A felnőttekben a legelterjedtebb hemoglobin-típus egy tetramer (négy fehérje alegységet tartalmaz), aminek a neve hemoglobin A. Ez két α és két β alegységet tartalmaz, ezek az alegységek 141 és 146 aminosavból épülnek fel. Összetétele α2β2. Az alegységek szerkezete hasonló és körülbelül azonos méretűek. Molekulatömegük 17 000 dalton körüli, a tetramer molekulatömege körülbelül 68 000 dalton. A hemoglobin A a legintenzívebben tanulmányozott hemoglobinmolekula. A láncokat ionos kötések, hidrogénhidak és hidrofób kölcsönhatások kapcsolják össze.
Szerepe
A szerkezetében lévő vasnak köszönhetően, a tüdőben megköti az oxigént és elszállítja a sejtekig. A sejtektől pedig a tüdőig a szén-dioxidot. Az oxigént megkötött hemoglobint oxihemoglobinnak nevezzük, a szén-dioxidot megkötött hemoglobint pedig carbohemoglobinnak.
Jegyzetek
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 60. o. ISBN 963 8334 96 7
Fordítás
Ez a szócikk részben vagy egészben a Hemoglobin című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.