Etilénglikol
A mai világban a Etilénglikol példátlan jelentőséggel bír a mindennapi élet különböző területein. A politikára gyakorolt hatásától a technológiára gyakorolt hatásáig a Etilénglikol jelenléte tagadhatatlan a globális színtéren. Ebben a cikkben megvizsgáljuk a Etilénglikol különböző dimenzióit, elemezve annak időbeli alakulását és a modern társadalomra gyakorolt hatását. Ezzel az elemzéssel jobban megérthetjük a Etilénglikol jelentőségét és szerepét a mai világ alakításában.
| Etilénglikol | |||

| |||
| |||
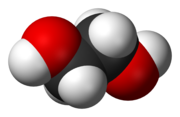
| IUPAC-név | Etán-1,2-diol | ||
| Más nevek | Etilénglikol Monoetilénglikol 1,2-dihidroxietán Glikol | ||
| Kémiai azonosítók | |||
| CAS-szám | 107-21-1 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C2H4(OH)2 | ||
| Moláris tömeg | 62,068 g/mol | ||
| Sűrűség | 1,1132 g/cm³ | ||
| Olvadáspont | −12,9 °C (260 K) | ||
| Forráspont | 197,3 °C (470 K) | ||
| Oldhatóság (vízben) | Vízzel minden arányban elegyedik. | ||
| Viszkozitás | 16,1 mPa s | ||
| Veszélyek | |||
| EU osztályozás | |||
| NFPA 704 | |||
| R mondatok | R22 | ||
| S mondatok | (S2) | ||
| Lobbanáspont | 111 °C (zárt csészében) | ||
| Öngyulladási hőmérséklet | 410 °C | ||
| LD50 | 4700 mg/kg (patkány, szájon át) | ||
| Rokon vegyületek | |||
| Rokon többértékű alkoholok | propilénglikol glicerin | ||
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |||
Az etilénglikol egy sűrűn folyó, édes ízű, mérgező folyadék. Fagyálló folyadékként használják. Egyszerűbb elnevezése a glikol. Szerves vegyület, a kétértékű alkoholok (diolok) legegyszerűbb képviselője.
Fizikai tulajdonságai
Az etilénglikol vagy monoetilénglikol (etán-1,2-diol) színtelen, sűrűn folyó, édes ízű, mérgező folyadék. A nagy viszkozitás oka az, hogy molekulái között erős hidrogénkötéseket alakít ki. Vízzel kiválóan elegyedik, de apoláris oldószerektől különválik. A molekula poláris részének hatása erősebb.
Felhasználása
A vízmolekulákkal erős hidrogénkötést képez, ami megakadályozza a szabályos jégkristályok kialakulását. Ennek eredményeképpen nagyon alacsony az olvadáspontja. 60%-os töménységű glikol -36 °C-on fagy meg. Ezért használják fagyálló folyadékként az autókban, épületgépészeti csőrendszerekben, vagy repülőgépek felületén végbemenő jégképződés ellen. Ezen kívül felhasználják még poliészter gyártásánál is.
Toxicitása
Az etilénglikol közepesen mérgező, embernél a minimális halálos dózis 1400 mg/testsúlykg, vagyis egy felnőtt esetében 75 ml, kb. fél pohárnyi. Veszélyességét az okozza, hogy édes ízű, ezért fennáll a nagyobb mennyiség elfogyasztásának veszélye. A fogyasztókhoz eljutó etilénglikol-tartalmú termékekbe (fagyálló) keserű ízt adó vegyületeket (denatónium-benzoát) ajánlott keverni.
A mérgezés első tünetei (30 perc-12 óra között) a központi idegrendszer működészavara, depressziója, ami szédülés, fejfájás, izomrángás formájában jelentkezik. A második fázisra (12-36 óra) felgyorsult légzés és szívdobogás jellemző. A harmadik fázisban (24-72 óra) vesetájéki fájdalom, véres vizelet, eleinte sok, aztán kevés vizelet jelzi a vese károsodását, ami kómához és halálhoz vezet.
A toxicitás kiváltója nem maga az etilénglikol, hanem a metabolitjai. Lebontásának első fázisában a máj alkohol-dehidrogenáz enzimje glikolaldehiddé alakítja (ezért a mérgezés ideiglenes ellenszere az etil-alkohol, amely lefoglalja ezt az enzimet), majd az aldehid-dehidrogenáz főleg glikolsavat és kisebb mértékben glioxált képez belőle. A mérgezés második fázisáért a glikolsav okozta elsavasodás felelős.
A glikolsav gyorsan lebomlik, főleg hangyasavra és szén-dioxidra, egy kisebb része (2,5%) viszont oxálsavvá alakul, amely kalcium-oxalát formájában kikristályosodik a vesében és ott szövetpusztulást és súlyos esetben a szerv teljes leállását okozza.
Az etilénglikol nagy dózisban patkányok esetében fejlődési rendellenességeket okoz az embriókban. Nyúlnál ilyen hatást nem sikerült megfigyelni, az ember esetében az ilyen hatások vitatottak.
Jegyzetek
- ↑ Elert, Glenn: Viscosity. The Physics Hypertextbook. (Hozzáférés: 2007. október 2.)
- ↑ a b c Etilénglikol (ESIS)[halott link]
- ↑ Az etilénglikol vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2010. december 28. (JavaScript szükséges) (angolul)
- ↑ Edward W. Carney: An Integrated Perspective on the Developmental Toxicity of Ethylene Glycol Reproductive Toxicology Vol 8. No 2. pp 99-113, 1994
